|
Молекула озона О3.
О3 –
голубоватый газ с сильным запахом, означает «пахучий»: в сосновых лесах его
много, у морского побережья, после грозы. Образуется из О2 под
действием УФ излучения и при грозовых разрядах:
3О2 = 2О3 (на свету)
Озон – сильнейший
окислитель, окислительная способность обусловлена нестойкостью его молекул,
которые при обычной температуре распадаются с образованием атомарного
кислорода, который активнее молекулы кислорода О2, на этом и
основано окислительное действие его . .
O3 ↔ O2 + O
Окисляет почти все
металлы, действуют на неметаллы, обесцвечивает красители, убивает микробы. При
высоких концентрациях – яд. (Один кислород имеет с.о. равную +4).Молекула имеет
угловое строение.
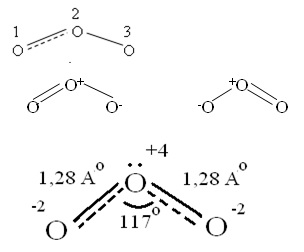
Связь
трехцентровая ( центральный атом О+4 находится в sp2-гибридизации,
связи его с двумя крайними атомами кислорода неравноценны, одна двойная, одна
одинарная).
Качественная реакция
на озон, крахмальная бумага, смоченная раствором KI
синеет в присутствии озона в результате выделения I2 ,озон более сильный
окислитель, чем О2 с ним эта реакция не протекает.
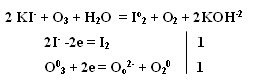
Земля окружена
слоем озона, располагающегося на высоте 25 км от её поверхности. Он
образуется за счёт поглощения кислородом ультрафиолетового излучения Солнца.
Озоновый слой ограничивает поток ультрафиолетового излучения, падающего на
землю. Увеличение интенсивности ультрафиолетового излучения, достигающего
Землю, могло бы привести к возрастанию заболеваний раком кожи. Вызывает беспокойство возможное
разрушение озонового слоя выхлопными газами реактивных самолётов. Сейчас этот
вопрос актуален и широко освещается в печати.
Химичесие
свойства О3
1. С
Металлами
Al + O3 →
Al2O3 + O2
2. Со сложными веществами
PbS + 2O3 →
PbSO4 + O2
3. Со щелочами
2 KOH + 7/3 O3 → O2 + 2KO3 + H2O
озонид калия
Кроме степени
окисления +4, кислород может проявлять степень окисления +2 в соединении со
фтором O+2F2 и +1 О2+1F2
2 F2 + 2 NaOH → 2NaF + O+2F2 + H2O-2
| 
