|
Общая характеристика элементов V-А группы
Главная подгруппа V группы периодической системы Д.И. Менделеева
включает пять элементов: типичные p-элементы азот N,
фосфор P, а также сходные с ними элементы больших периодов мышьяк
As, сурьму Sb, и висмут Bi.
Они имеют общее название пниктогены. Атомы этих элементов имеют на
внешнем уровне по 5 электронов (конфигурация ns2 np3).
В соединениях элементы проявляют степень
окисления от -3 до +5. Наиболее характерны степени +3 и +5. Для висмута более характерна степень
окисления +3.
При переходе от N
к Bi радиус атома закономерно возрастает. С увеличением
размеров атомов уменьшается энергия ионизации. Это значит, что связь электронов
наружного энергетического уровня с ядром у атомов ослабевает, что приводит к
ослаблению неметаллических и усилению металлических свойств в ряду от азота к Bi.
Азот и фосфор –
типичные неметаллы, т.е. кислотообразователи. У мышьяка сильнее выражены
неметаллические свойства. У сурьмы неметаллические и металлические свойства проявляются
приближенно в одинаковой степени. Для висмута характерно преобладание
металлических свойств.
У
атома азота три неспаренных электрона. Поэтому валентность азота равна трем.
Из-за отсутствия у него d-подуровня на внешнем
уровне его электроны разъединиться не могут. Однако в результате
донорно-акцепторного взаимодействия азот становится четырехвалентным.
У атомов фосфора и
последующих элементов VА группы имеются
свободные орбитали на d-подуровне и переходя
в возбужденное состояние будут разъединятся 3s-электроны.
В невозбужденном состоянии у всех элементов 5А группы валентность равна 3, а в
возбужденном состоянии всех, кроме
азота, равна пяти.
Элементы этой группы
образуют газообразные водородные соединения (гидриды) типа ЭН3 , в
которых степень их окисления -3.
NH3 аммиак
PH3 фосфин
AsH3 арсин
SbH3 стибин
BiH3 висмутин
AsH3, SbH3 газы с неприятным
запахом, легко разлагаются. Чрезвычайно ядовиты.
В
кислородных соединениях для элементов VА группы наиболее
характерны степени окисления +3 и +5. Для висмута более характерна степень
окисления +3.
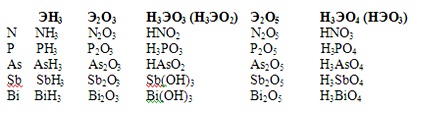
Все
элементы VА группы имеют оксиды типа Э2О5 и
гидроксиды НЭО3 или Н3ЭО4 , которые обладают
кислотными свойствами. Кроме того для них характерны оксиды типа Э2О3
и соответствующие гидроксиды НЭО2 или Н3ЭО3 ,
у азота и фосфора они имеют кислотные свойства, у мышьяка и сурьмы – амфотерные,
а у висмута проявляют основной характер.
Характерно также образование галидов типа ЭГ3
(тригалиды), которые (за исключением NF3) гидролизуются по схеме:
ЭГ3 + 3Н2О = Н3ЭО3
+ 3НГ
ЭCl3 + H2O = H3ЭО3 + 3НCl
но в
присутствии галоводородной кислоты галиды сурьмы и висмута гидролизуются с
образованием галоксидов, например
SbCl3 + H2O = SbOCl + 2HCl
Группу SbO+ называют антимонилом, а соединение SbOCl – хлоридом антимонила. Для фосфора, мышьяка и сурьмы
известны пентафториды ЭF5 , а для фосфора и сурьмы пентахлориды ЭCl5.
Мышьяк и сурьма имеют ряд аллотропных
форм. Наиболее устойчивые металлические формы серого (As) и серебристо-белого (Sb) цвета. Это хрупкие
вещества, легко превращаемые в порошок. Висмут – металл серебристо-белого цвета
с едва заметным розовым оттенком.
Соединения As, Sb, Bi ядовиты. Особо опасны соединения As3+ ( AsH3-
арсин).
| 
